Energetski pojasevi
metali
Valenski elektroni koji u drugim tvarima stvaraju vezu između pojedinih atoma ili malih skupina atoma dijele se jednaki na sve atome u komadu metala. Ti delokalizirani elektroni mogu se pomicati preko cijelog komada metala i pružati metalni sjaj i dobru električnu i toplinsku provodljivost metala i legura. Teorija bendova objašnjava da su u takvom sustavu pojedinačne razine energije zamijenjene neprekidnom regijom koja se naziva opsegom, kao na dijagramu gustoće stanja metala bakra prikazanom na slici. Ovaj dijagram pokazuje da broj elektrona koji se mogu smjestiti u pojasu u bilo kojoj energiji varira; u bakru se broj smanjuje kako se bend približava ispunjavajući se elektronima. Broj elektrona u bakru ispunjava pojas do prikazane razine, ostavljajući neki prazan prostor pri višim energijama.
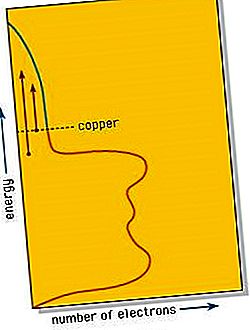
Kad foton svjetlosti apsorbira elektron blizu vrha energetskog pojasa, elektron se podiže na višu dostupnu razinu energije unutar pojasa. Svjetlost se tako intenzivno apsorbira da može prodrijeti do dubine od samo nekoliko stotina atoma, obično manju od jedne valne duljine. Budući da je metal provodnik električne energije, ta apsorbirana svjetlost, što je na kraju krajeva, i elektromagnetski val, inducira izmjenične električne struje na metalnoj površini. Ove struje odmah otpuštaju foton iz metala, pružajući tako snažan odraz polirane metalne površine.
Učinkovitost ovog postupka ovisi o određenim pravilima odabira. Ako je učinkovitost apsorpcije i ponovnog smanjivanja približno jednaka pri svim optičkim energijama, tada će se različite boje u bijeloj svjetlosti odraziti jednako dobro, što dovodi do „srebrnaste“ boje poliranog srebra i željeza. U bakru se učinkovitost refleksije smanjuje s povećanjem energije; smanjena reflektivnost na plavom kraju spektra rezultira crvenkastom bojom. Slična razmatranja objašnjavaju žutu boju zlata i mjedi.
Čisti poluvodiči
U većini tvari pojavljuje se jaz u pojasu u dijagramu gustoće stanja (vidi sliku). To se može dogoditi, na primjer, kada u čistoj tvari postoji prosječno točno četiri valentna elektrona po atomu, što rezultira potpuno potpunim donjim pojasom, nazvanim valentni pojas, i točno praznim gornjim pojasom, provodnim vrhom. Budući da u razmaku između dvaju područja nema razine energije elektrona, najniža energetska svjetlost koja se može apsorbirati odgovara strelici A na slici; to predstavlja pobudu elektrona od vrha valentne trake do dna vodljivog pojasa i odgovara energiji zazora između grede označenoj E g. Svjetlost bilo koje veće energije također se može apsorbirati, što pokazuju strelice B i C.
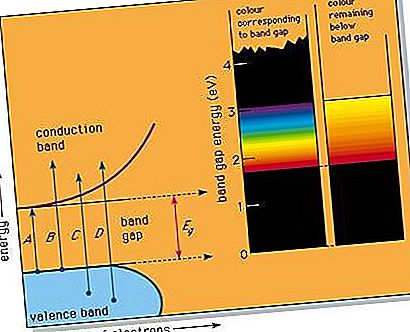
Ako tvar ima veliki razmak, poput 5,4 eV dijamanta, tada se svjetlost u vidljivom spektru ne može apsorbirati, a tvar se čini bezbojnom kad je čista. Takvi poluvodiči s velikim razmakom su izvrsni izolatori i najčešće se tretiraju kao ionski ili kovalentno vezani materijali.
Pigment kadmij žuti (kadmij sulfid, također poznat kao mineral greenockit) ima manji razmak od 2,6 eV, što omogućava apsorpciju ljubičaste i neke plave, ali nijedne druge boje. To dovodi do njegove žute boje. Nešto manji jaz koji dopušta apsorpciju ljubičaste, plave i zelene boje daje narančastu boju; još manji razmak pojasa kao u 2.0 eV pigmentnog vermiliona (živin sulfid, mineralni cinobar) rezultira svim energijama, ali crvena se apsorbira, što dovodi do crvene boje. Sva se svjetlost apsorbira kada je energija zazora pojasa manja od 1,77-eV (700 nm) granice vidljivog spektra; poluvodiči s uskim razmakom, poput galene olovnog sulfida, apsorbiraju svu svjetlost i crni su. Ovaj niz bezbojnih, žutih, narančastih, crvenih i crnih boja je precizan raspon boja dostupan u čistim poluvodičima.
Doped poluvodiči
Ako je atom nečistoće, često nazvan dopant, prisutan u poluvodiču (koji je tada označen kao dopiran) i ima različit broj valentnih elektrona od atoma koji zamjenjuje, u razmaku pojasa mogu se formirati dodatne razine energije. Ako nečistoća sadrži više elektrona, poput onečišćenja dušika (pet valentnih elektrona) u dijamantskom kristalu (koji se sastoji od ugljika, od kojih svaki ima četiri valentna elektrona), formira se razina donora. Elektroni s ove razine mogu se pobuditi u kondukcijski pojas apsorpcijom fotona; to se događa samo na plavom kraju spektra u dijamantu dušenom dušikom, što rezultira komplementarnom žutom bojom. Ako nečistoća ima manje elektrona od atoma koji zamjenjuje, poput nečistoće bora (tri valentna elektrona) u dijamantu, formira se razina rupe. Fotoni se sada mogu apsorbirati uzbuđenjem elektrona iz valentnog pojasa u razinu rupe. Kod dijamanta koji je dopiran borom događa se samo na žutom dijelu spektra, što rezultira dubokom plavom bojom kao u poznatom Hopeovom dijamantu.
Neki materijali koji sadrže i donore i akceptore mogu apsorbirati ultraljubičastu ili električnu energiju za proizvodnju vidljive svjetlosti. Na primjer, fosforni prahovi, poput bakra koji sadrži cink sulfid i druge nečistoće, koriste se kao prevlaka u fluorescentnim svjetiljkama za pretvaranje obilne ultraljubičaste energije koju proizvodi živin luk u fluorescentnu svjetlost. Fosfor se koristi i za premazivanje unutrašnjosti televizijskog ekrana, gdje se aktiviraju strujom elektrona (katodne zrake) u katodoluminiscenciji i u svjetlosnim bojama gdje ih aktivira bijela svjetlost ili ultraljubičasto zračenje, što ih uzrokuje prikazuju spor svjetlosni raspad poznat kao fosforescencija. Elektroluminescencija nastaje kao posljedica električnog uzbuđenja, kao kad se fosforni prah taloži na metalnu ploču i prekriva prozirnom elektrodom za proizvodnju rasvjetnih ploča.
Injekciona elektroluminescencija nastaje kada kristal sadrži spoj između različito dopiranih poluvodičkih područja. Električna struja stvorit će prijelaze između elektrona i rupa u području spajanja, oslobađajući energiju koja se može pojaviti kao gotovo jednobojna svjetlost, kao u diodama (LED) koje emitiraju svjetlost, a koje se široko koriste na uređajima za prikaz u elektroničkoj opremi. S pogodnom geometrijom, emitirano svjetlo također može biti jednobojno i koherentno kao u poluvodičkim laserima.