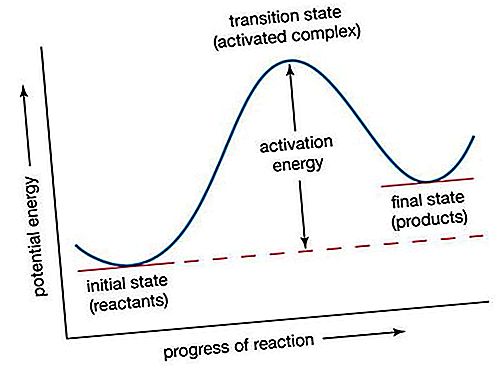
Rodij (Rh), kemijski element, jedan od platinskih metala skupine 8–10 (VIIIb), razdoblja 5 i 6, periodičke tablice, pretežno korišten kao legirajući agens za očvrsnuće platine. Rhodium je dragocjen, srebrno bijeli metal, s visokom reflektivnošću na svjetlost. Atmosfera ne korodira i ne smeta pri sobnoj temperaturi, a često se nanosi na metalne predmete i polira kako bi se dobile trajne, atraktivne površine za nakit i druge ukrasne predmete. Metal se također koristi za proizvodnju reflektirajućih površina za optičke instrumente.
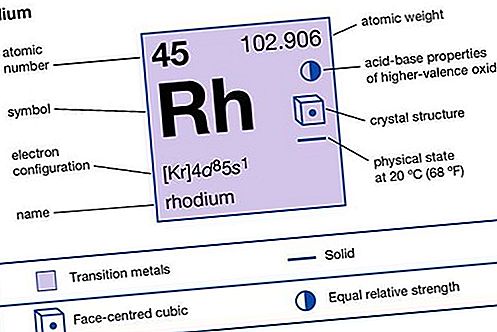
Rodij dodan platini u malim količinama daje legure koje su tvrđe i gube težinu na visokim temperaturama još sporije od čiste platine. Takve se legure koriste za laboratorijske peći, elektrode sa svjećicama i katalizatore u vrlo vrućim kemijskim okruženjima (uključujući automobilske katalitičke pretvarače). U industrijskoj proizvodnji dušične kiseline koriste se gazni katalizatori rodij-platinske legure jer mogu izdržati temperaturu plamena jer se amonijak sagorijeva u dušikov oksid. Žica od legure 10 posto rodio-90 posto platine spojena s žicom od čiste platine čini izvrstan termoelement za mjerenje visokih temperatura u oksidirajućoj atmosferi. Međunarodna temperaturna ljestvica definirana je u području od 660 ° do 1,063 ° C (1,220 ° do 1,945 ° F) pomoću elektromotorne sile ovog termoelementa.
Rodij je rijedak element koji sadrži do 4,6 posto nativnih legura platine. Javlja se i u urođenim legurama iridija i osmija: do i 11,25 posto u iridosminu i do najmanje 4,5 posto u siserskitu. Rhodium se javlja u prirodi zajedno s ostalim metalima platine, a njegovo razdvajanje i pročišćavanje čine dio cjelokupne metalurške prerade skupine. Rodij se općenito komercijalno dobiva kao nusproizvod ekstrakcije nikla i bakra iz njihovih ruda.
Prirodni rodijum sastoji se u cijelosti od stabilnog izotopa rodija-103. Element je prvi izolirao (1803.) iz sirove platine engleski kemičar i fizičar William Hyde Wollaston, koji ga je nazvao grčkim rodonom ("ružom") zbog crvene boje niza njegovih spojeva. Rhodium je vrlo otporan na napade kiselina; masivni metal se ne rastvara vrućom koncentriranom dušičnom ili klorovodičnom kiselinom ili čak akva-regije. Metalni otapa u kondenziranog kalij hidrogen sulfata, čime se dobije kompleks, u vodi topljivi sulfata K 3 Rh (SO 4) 3 · 12H 2 O, u vrućem koncentrirane sumporne kiseline, te je u koncentriranoj klorovodičnoj kiselini koja sadrži natrijev perklorat na 125 ° -150 ° C (257 ° -302 ° F).
Rodijeva se kemija koncentrira uglavnom na oksidacijska stanja +1 i +3; prepoznaje se nekoliko spojeva ostalih pozitivnih oksidacijskih stanja kroz +6. Rodij formira dirhodium tetraacetatom, Rh 2 (O 2 CCH 3) 4 i različiti derivati sadrže dva liganda-primjerice, voda, piridin ili trifenilfosfin-u oksidacijskom stanju +2. Kompleksi u oksidacijskom stanju +1 uglavnom sadrže ugljični monoksid, olefine i fosfine kao ligande. Svi rodijevi spojevi se lako smanjuju ili razgrađuju zagrijavanjem, čime se dobiva metal u prahu ili spužvi. Među tim spojevima rodij triklorid, RhCI 3 (u kojem je rodij +3 stanja), je jedan od najvažnijih. Omogućuje početni materijal za mnoge druge rodijeve spojeve u različitim oksidacijskim stanjima. U vodenim emulzijama može katalizirati brojne korisne organske reakcije.
Svojstva elementa
| atomski broj | 45 |
|---|---|
| atomska težina | 102,905 |
| talište | 1.966 ° C (3.571 ° F) |
| vrelište | 3.727 ° C (6.741 ° F) |
| specifična gravitacija | 12,4 (20 ° C) |
| oksidacijska stanja | +1, +2, +3, +4, +5, +6 |
| konfiguracija elektrona. | [Kr] 4d 8 5s 1 |