Radij (Ra), radioaktivni kemijski element, najteži od zemnoalkalnih metala grupe 2 (IIa) periodičke tablice. Radij je srebrnasto bijeli metal koji se u prirodi ne pojavljuje besplatno.
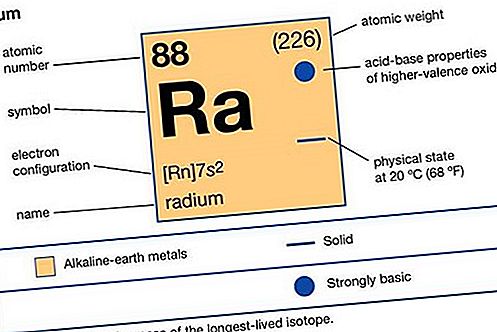

zemnoalkalijski metal
barij (Ba) i radijum (Ra).
Svojstva elementa
| atomski broj | 88 |
|---|---|
| najstabilniji izotop | 226 |
| talište | oko 700 ° C (1.300 ° F) |
| vrelište | nije dobro utvrđen (oko 1.100–1.700 ° C [2.000–3.100 ° F]) |
| specifična gravitacija | oko 5 |
| oksidacijsko stanje | 2 |
| konfiguracija elektrona | [Rn] 7s 2 |
Pojava, svojstva i upotrebe
Radij su otkrili Pierre Curie, Marie Curie i njegov pomoćnik, G. Bémont, nakon što je Marie Curie primijetila da je radioaktivnost pitchblende četiri ili pet puta veća od one urana koju je sadržavao i nije u potpunosti objašnjena osnova radioaktivnog polonija, koju je upravo otkrila u ostacima smolende. Nova, snažno radioaktivna tvar mogla bi se koncentrirati s barijem, ali, budući da je njegov klorid bio malo netopljiviji, mogao se istaložiti frakcijskom kristalizacijom. Odvajanju je pratio porast intenziteta novih linija u ultraljubičastom spektru i stalni porast prividne atomske težine materijala sve dok se ne dobije vrijednost 225,2, što je znatno blizu trenutno prihvaćenoj vrijednosti 226,03. Do 1902. pripravljeno je 0,1 grama čistog radijum-klorida rafiniranjem nekoliko tona ostataka smole, a do 1910. Marie Curie i André-Louis Debierne izolirali su metal.
Poznato je trideset četiri izotopa radija, svi radioaktivni; njihov poluživot, osim radijuma-226 (1.600 godina) i radija-228 (5.75 godina), kraći su od nekoliko tjedana. Dugovječni radij-226 nalazi se u prirodi kao rezultat kontinuiranog stvaranja od propadanja urana-238. Radij se, dakle, pojavljuje u svim uranovim rudama, ali je rašireniji jer tvori u vodi topljive spojeve; Zemljina površina sadrži procijenjenih 1,8 × 10 13 grama (2 × 10 7 tona) radijusa.
Budući da su svi izotopi radijuma radioaktivni i kratkotrajni su na geološkoj vremenskoj skali, bilo koji prvobitni radijus već bi odavno nestao. Stoga se radij javlja prirodno samo kao produkt raspadanja u tri prirodne serije raspada (torij, uran i aktinij). Radium-226 član je serije propadanja urana. Roditelj mu je torij-230, a kćer radon-222. Daljnji produkti raspadanja, prethodno zvani radijus A, B, C, C ′, C ″, D, i tako dalje, su izotopi polonija, olova, bizmuta i talija.