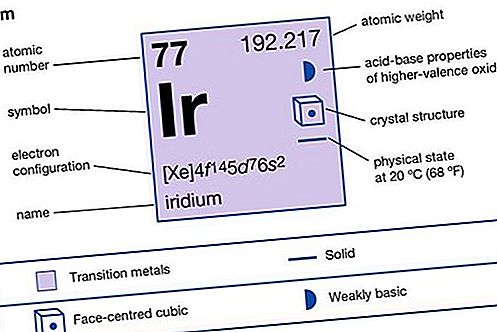
Iridium (Ir), kemijski element, jedan od platinskih metala skupina 8–10 (VIIIb), razdoblja 5 i 6, periodičke tablice. Vrlo je gusta i rijetka te se koristi u legurama platine. Plemeniti, srebrno bijeli metal, iridij je tvrd i lomljiv, ali postaje dukantan i može se raditi na bijeloj vrućini, od 1.200 ° do 1.500 ° C (2.200 ° do 2.700 ° F). To je jedna od najgušćih kopnenih tvari. U masivnom je stanju metal praktično netopljiv u kiselinama, a ne napada ga ni akvaregija. Može se otopiti u koncentriranoj klorovodičnoj kiselini u prisutnosti natrijevog perklorata na 125 ° do 150 ° C (257 ° do 302 ° F).
Zbog poteškoća u pripremi i proizvodnji, čisti metal ima malo primjene. Iridij se uglavnom koristi u obliku legura platine. Legura platine-iridija (5 do 10 posto iridija) metali su koji su lako obradivi, a koji su mnogo tvrđi i čvršći i otporniji na kemijski napad od meke čiste platine. Takve se legure koriste za nakit, olovke, kirurške igle i osovine te električne kontakte i iskre. Međunarodni prototip standardnih kilograma mase izrađen je od legure koja sadrži 90 posto platine i 10 posto iridija.
Čisti iridij se vjerojatno ne pojavljuje u prirodi; njegovo je bogatstvo u Zemljinoj kori vrlo malo, oko 0,001 dijelova na milijun. Iako je rijedak, iridij se pojavljuje u prirodnim legurama s drugim plemenitim metalima: u iridosminu do 77 posto iridija, u platiniridijumu do 77 posto, u aurosmiridijumu 52 posto, a u nativnoj platini do 7,5 posto. Iridij se obično proizvodi komercijalno zajedno s ostalim metalima platine kao nusproizvod proizvodnje nikla ili bakra.
Rude koje sadrže iridij nalaze se u Južnoj Africi i na Aljasci, u SAD-u, kao i u Mjanmaru (Burmi), Brazilu, Rusiji i Australiji. Južna Afrika je krajem 20. stoljeća bila glavni svjetski proizvođač iridija.
Engleski je kemičar Smithson Tennant otkrio taj element 1803. godine u kiselinama netopljivim ostacima platinskih ruda; francuski kemičari H.-V. Collet-Descotils, A.-F. Fourcroy, i N.-L. Vauquelin je identificirao otprilike u isto vrijeme. Naziv iridium, izveden iz grčke riječi iris ("duga"), odnosi se na različite boje njegovih spojeva. Prirodni iridij sastoji se od mješavine dva stabilna izotopa, iridijuma-191 (37,3 posto) i iridija-193 (62,7 posto). Kemija iridija usredotočuje se na oksidacijska stanja +1, +3 i +4, iako su poznati spojevi svih stanja od 0 do +6, s iznimkom +2. Kompleksi u oksidacijskom stanju +1 uglavnom sadrže ugljični monoksid, olefine i fosfine kao ligande. Anionski heksakloroiridat, [IrCl 6] 2- i heksabromoiridat, [IrBr 6] 2−, jedine su zapažene kemijske vrste koje sadrže iridij u stanju oksidacije +4. Iridij je nešto reaktivniji od rutenija i osmija.
Svojstva elementa
| atomski broj | 77 |
|---|---|
| atomska težina | 192,2 |
| talište | 2.410 ° C |
| vrelište | 4,527 ° C (8,181 ° F) |
| specifična gravitacija | 22,4 (20 ° C) |
| oksidacijska stanja | +1, +3, +4 |
| konfiguracija elektrona. | [Xe] 4f 14 5d 9 |