Oksiacid, bilo koja kiselina koja sadrži kisik. Većina kovalentnih nemetalnih oksida reagira s vodom i formira kisele okside; to jest, reagira s vodom da se dobije prinos oksikiselina koje hydronium ioni (H 3 O +) u otopini. Postoje neke iznimke, kao što su ugljični monoksid, CO, dušikov oksid, N- 2, O i dušičnog oksida NO.
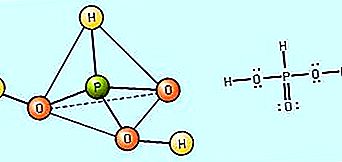
Jačina oksidacida definirana je stupnjem disocijacije u vodi (tj. Njegovom sposobnošću formiranja H + iona). Općenito, relativna snaga oksidacida može se predvidjeti na osnovi elektronegativnosti i oksidacijskog broja središnjeg nemetalnog atoma. Jačina kiseline povećava se kako raste elektronegativnost središnjeg atoma. Na primjer, budući da Elektronegativnost klora (Cl) je veća od sumpora (S), koja je zauzvrat veća od fosfora (P), može se predvidjeti da perklornom kiselinom, HCIO 4, je jače kiseline od sumporna kiselina, H 2 SO 4, koji bi trebao biti jače kiseline od fosforne kiseline, H 3 PO 4, Za određeni nemetalni središnji atom, jačina kiseline raste kako se povećava oksidacijski broj središnjeg atoma. Na primjer, dušična kiselina, HNO 3, u kojima je dušik (N) ima atom oksidacijski broj +5 je jače kiseline od dušičnom kiselinom, HNO 2, gdje je oksidacijsko stanje je dušik +3. Na isti način, sulfatna kiselina, H 2 SO 4, sa sumporom u svom +6 oksidacijskom stanju, je jače kiseline od sumporaste kiseline, H 2 SO 3, gdje postoji niz +4 oksidacija sumpora.
Sol oksidacida je spoj koji nastaje kada kiselina reagira s bazom: kiselina + baza → sol + voda. Ova vrsta reakcije naziva se neutralizacija, jer se otopina čini neutralnom.