Dušična kiselina, (HNO 3), bezbojna, dimna i jako korozivna tekućina (tačka smrzavanja -42 ° C [-44 ° F], tačka ključanja 83 ° C [181 ° F]) koja je uobičajeni laboratorijski reagens i važan industrijska kemikalija za proizvodnju gnojiva i eksploziva. Toksičan je i može izazvati teške opekotine.
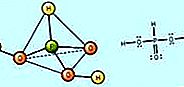
oksidacid: soli dušične kiseline i nitrati
Dušična kiselina, HNO3, alkemičarima 8. stoljeća bila je poznata kao "aqua fortis" (jaka voda). Formira se
Priprema i upotreba dušične kiseline bila je poznata ranim alhemičarima. Dugogodišnji uobičajeni laboratorijski postupak, pripisan njemačkom kemičaru Johannu Rudolfu Glauberu (1648.), sastojao se od zagrijavanja kalijevog nitrata koncentriranom sumpornom kiselinom. Antoan-Laurent Lavoisier je 1776. pokazao da sadrži kisik, a 1816. Joseph-Louis Gay-Lussac i Claude-Louis Berthollet utvrdili su njegov kemijski sastav.
Glavna metoda proizvodnje dušične kiseline je katalitička oksidacija amonijaka. U metodi koju je 1901. godine razvio njemački kemičar Wilhelm Ostwald, plin amonijaka se oksidira u dušikov oksid i dušikov dioksid zrakom ili kisikom u prisutnosti katalizatora platinske gaze. Dušikov dioksid se apsorbira u vodi kako bi tvorio dušičnu kiselinu. Rezultirajuća otopina kiselina u vodi (oko 50 do 70 mas.% Kiseline) može se dehidrirati destilacijom sa sumpornom kiselinom.
Dušična kiselina se razgrađuje u vodi, dušičnom dioksidu i kisiku, formirajući smećkastu žutu otopinu. To je jaka kiselina, potpuno ionizirane u hydronium (H 3 O +) i nitrata (NO 3 -) iona u vodenoj otopini, te snažno oksidacijsko sredstvo (onaj koji djeluje kao akceptor elektrona u reakcijama oksidacije-redukcije). Među mnogim važnim reakcijama dušične kiseline su: neutralizacija amonijakom kako bi nastao amonijev nitrat, glavna komponenta gnojiva; nitriranje glicerola i toluena, tvoreći eksplozive nitroglicerin i trinitrotoluen (TNT), respektivno; priprema nitroceluloze; i oksidaciju metala odgovarajućim oksidima ili nitratima.